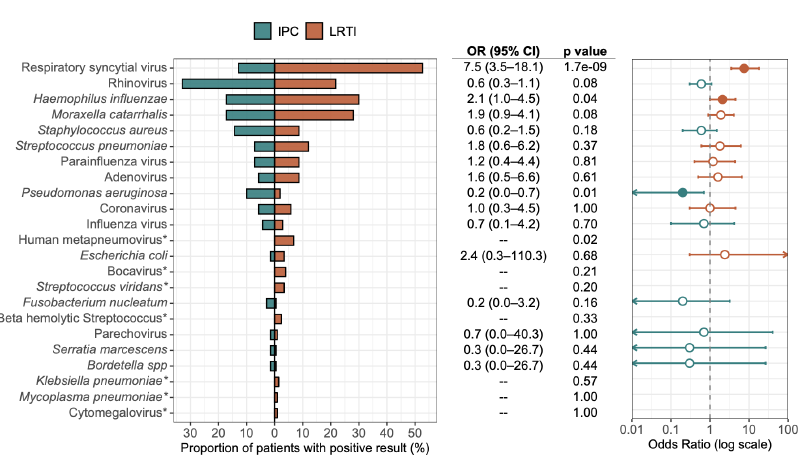
背景
呼吸道微生物组中常存在具有致病潜力的微生物(Pathobionts),它们可能在气道中处于无症状携带状态(IPC),而不引起感染症状和体征。IPC 的存在严重干扰了急性呼吸道疾病的临床诊断,因为传统的病原检测无法区分是“真感染”还是“单纯携带”,这往往导致抗菌药物的滥用或漏诊非感染性病因。尽管 IPC 在各年龄段均有发生,但在儿童中尤为普遍(如肺炎链球菌携带率可达 33-90%)。目前,尚缺乏能够准确区分 LRTI 与 IPC 的有效检测手段,且两者背后的宿主-微生物相互作用机制尚不明确。
- Lydon, E. C., Deosthale, P., Glascock, A., et al. (2026). Host-microbiome archetypes differentiate infection from pathogen carriage in the human lower airway. Nature Communications.
- 期刊:Nature Communications (IF 15.7)
- 发表时间:2026年4月13日
本研究通过对 326 名机械通气儿童的气管抽吸物进行宿主-微生物宏转录组分析,发现 LRTI 表现为气道微生物组 Alpha 多样性降低、代谢活性改变以及强烈的先天/适应性免疫激活;而 IPC 则表现为微生物多样性丰富、代谢活跃但宿主转录谱与未感染对照组相似。基于 FABP4 基因(编码巨噬细胞相关脂质伴侣)结合 Alpha 多样性的分类器,能准确区分 LRTI 与 IPC(AUC=0.89),单独的 FABP4 蛋白检测亦表现出色(AUC=0.88)。这表明整合宿主与微生物特征可实现对 LRTI 的数据驱动型精准诊断。
方法
研究人员对 457 名因急性呼吸衰竭接受机械通气的儿童进行了前瞻性队列研究。在插管后 24 小时内收集气管抽吸物(Tracheal Aspirates),并提取 RNA 进行宏转录组测序,最终纳入 343 名患者数据。
研究通过至少两名医生的盲法临床裁定,将患者分为三组:确诊 LRTI 且有病原体检出(LRTI组,n=207)、非感染性呼吸衰竭但有病原体检出(IPC组,n=70)、非感染性呼吸衰竭且无病原体检出(对照组 CTRL,n=49)。
数据分析涵盖了微生物组(Alpha/Beta 多样性、差异丰度分析 ANCOM-BC、毒力因子及代谢通路 HUMAnN)和宿主转录组(差异表达分析、GSEA 富集分析)。此外,研究还构建了基于 LASSO 回归的诊断分类器,并进行了中介分析以探讨微生物组对宿主免疫应答的调节作用。
结果
下呼吸道微生物组的生态差异
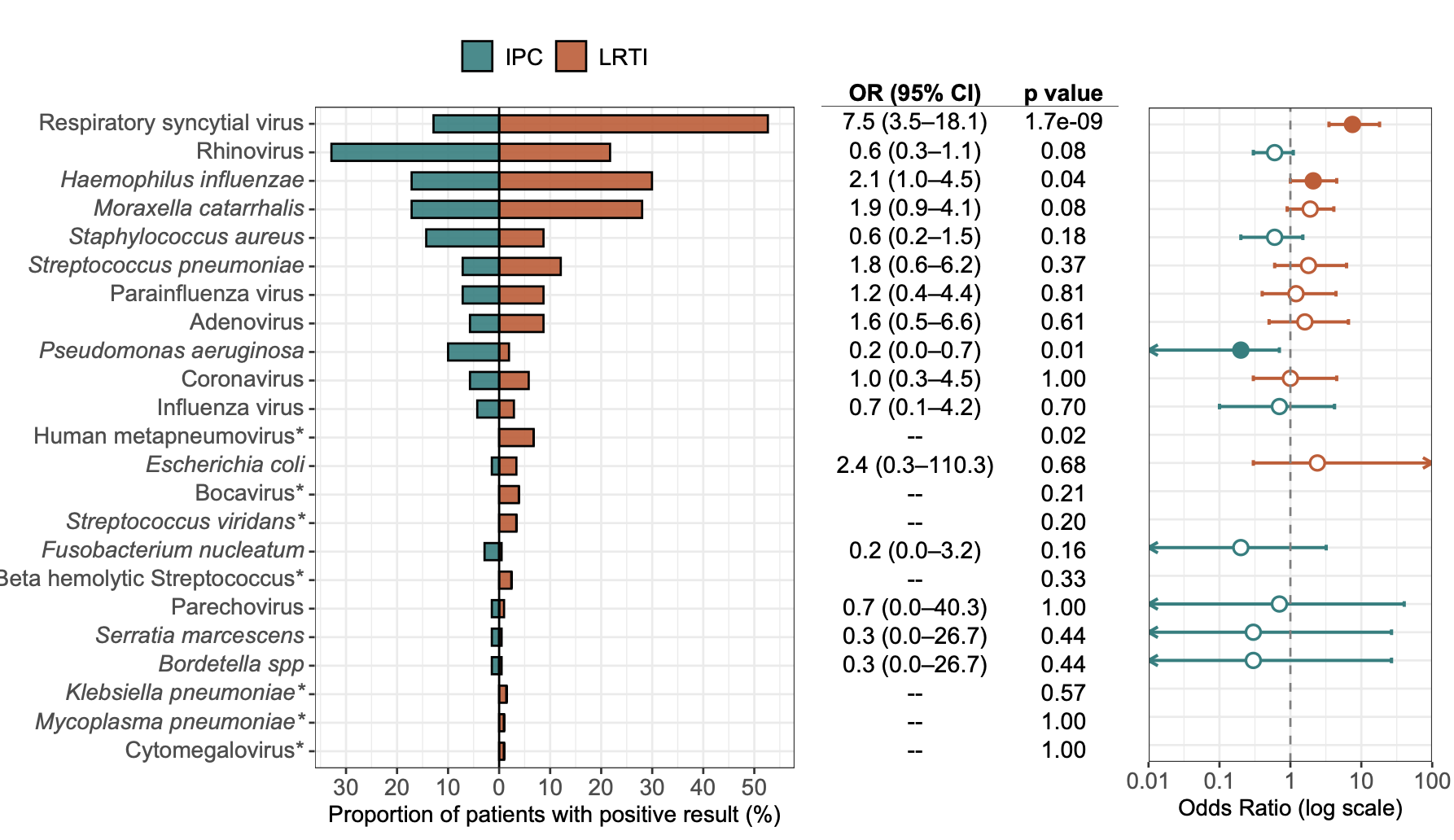
微生物组分析显示,LRTI 患者的气道微生物组 Alpha 多样性(Shannon Index)显著低于 IPC 组和 CTRL 组,且物种丰富度也更低。相反,IPC 组的总细菌丰度(RPM)实际上高于 LRTI 组。在分类学上,IPC 组富集了普雷沃氏菌属(Prevotella)、奈瑟菌属(Neisseria)等经典共生菌和厌氧菌;而 LRTI 组仅呼吸道合胞病毒(RSV)显著富集。功能分析发现,IPC 状态下微生物的代谢通路(如脂肪酸β-氧化、精氨酸降解)更为活跃,且流感嗜血杆菌的毒力因子(如粘附素 HMW1/2)在 LRTI 中表达更高。
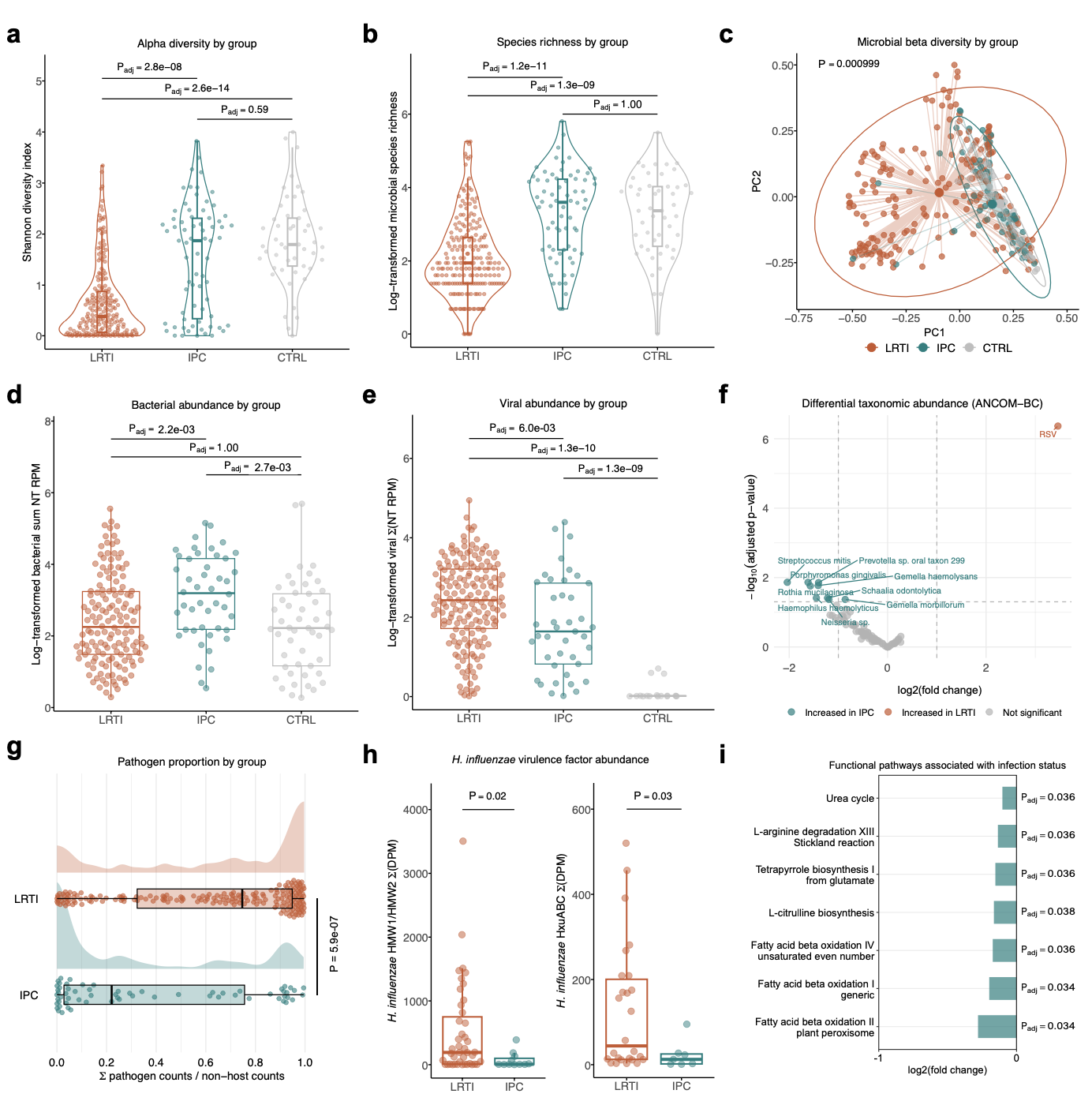
宿主免疫应答的转录组特征
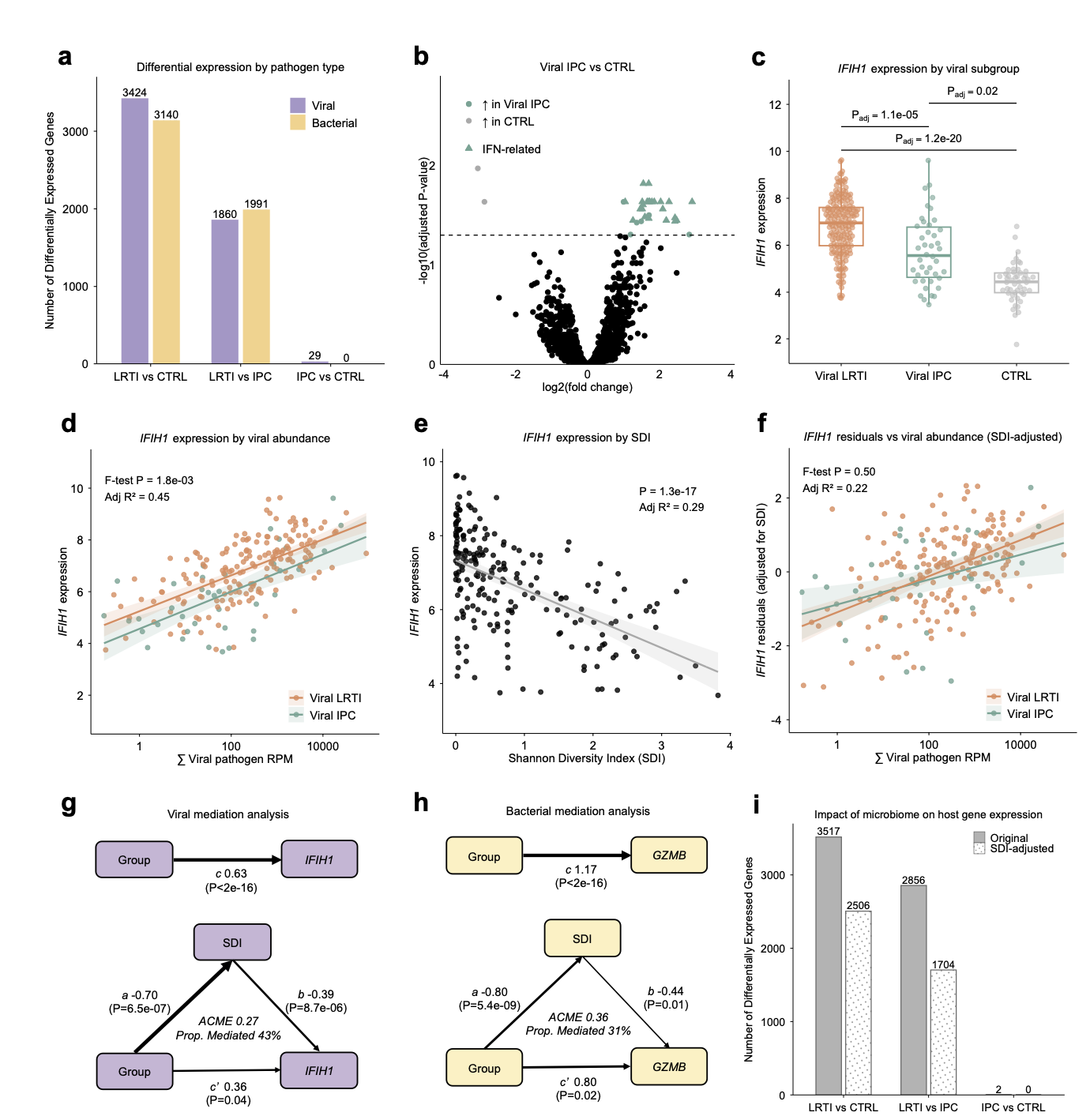
宿主转录组分析表明,LRTI 患者具有独特的免疫激活特征,涉及干扰素信号、抗原呈递和中性粒细胞脱颗粒等通路的上调,与 IPC 或 CTRL 组存在显著差异(3517 个差异基因)。相比之下,IPC 组的转录谱与未感染对照组极为相似(仅 2 个差异基因)。值得注意的是,FABP4(脂肪酸结合蛋白 4,一种巨噬细胞相关的脂质伴侣)在 LRTI 中表达显著上调,是区分感染状态的关键 outlier 基因。
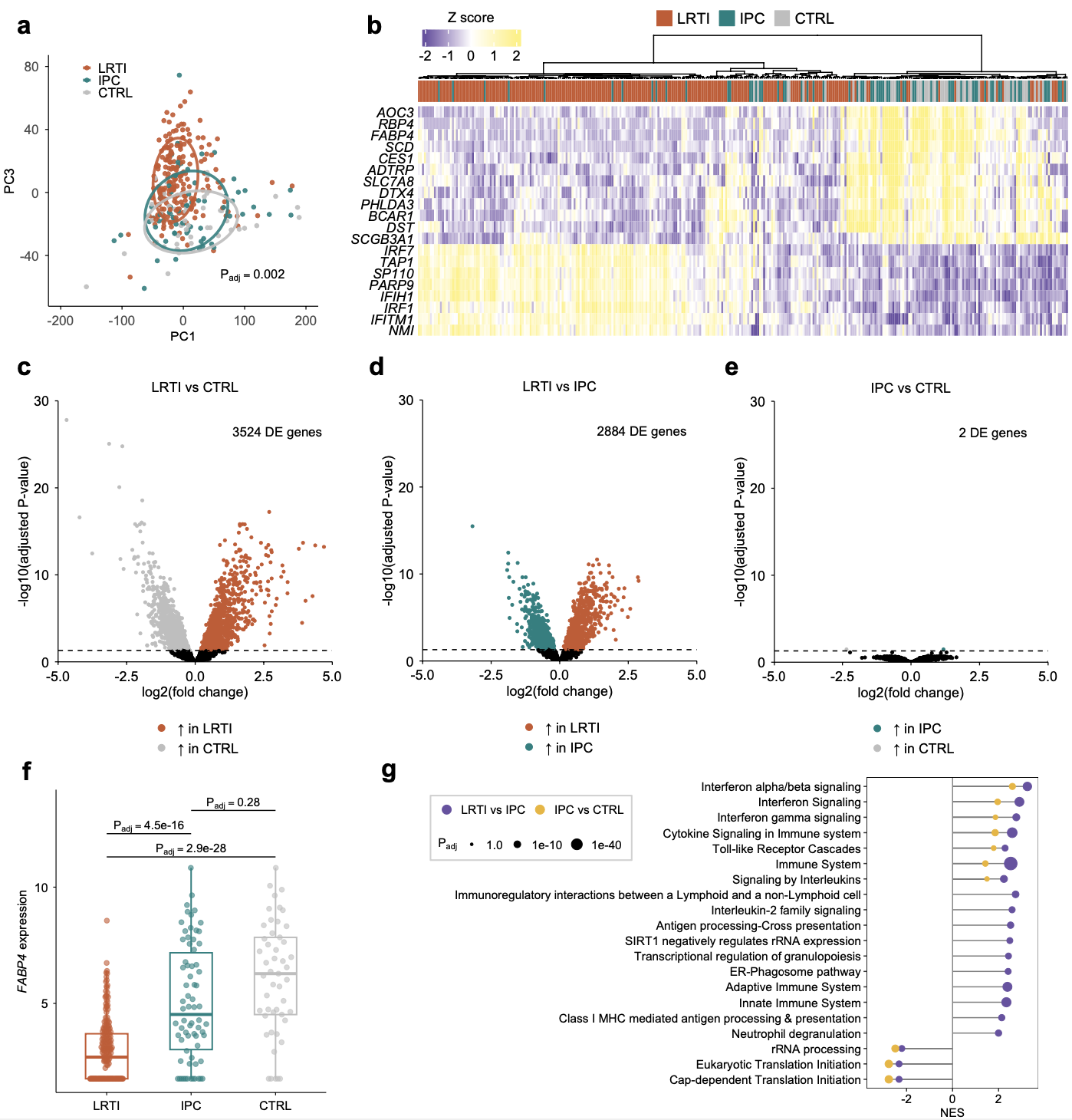
病毒与细菌携带的免疫异质性
细分分析发现,病毒 IPC 会诱导微弱的干扰素刺激基因(ISG)表达,而细菌 IPC 则完全未引起明显的转录组变化。回归分析显示,虽然 ISG 表达与病毒载量正相关,但在相同病毒载量下,IPC 患者的 ISG 反应强度显著低于 LRTI 患者(即存在“应答衰减”现象)。此外,中介分析表明,较低的微生物 Alpha 多样性与较高的 ISG 表达独立相关,暗示微生物组结构可能调节宿主对病毒的免疫反应。
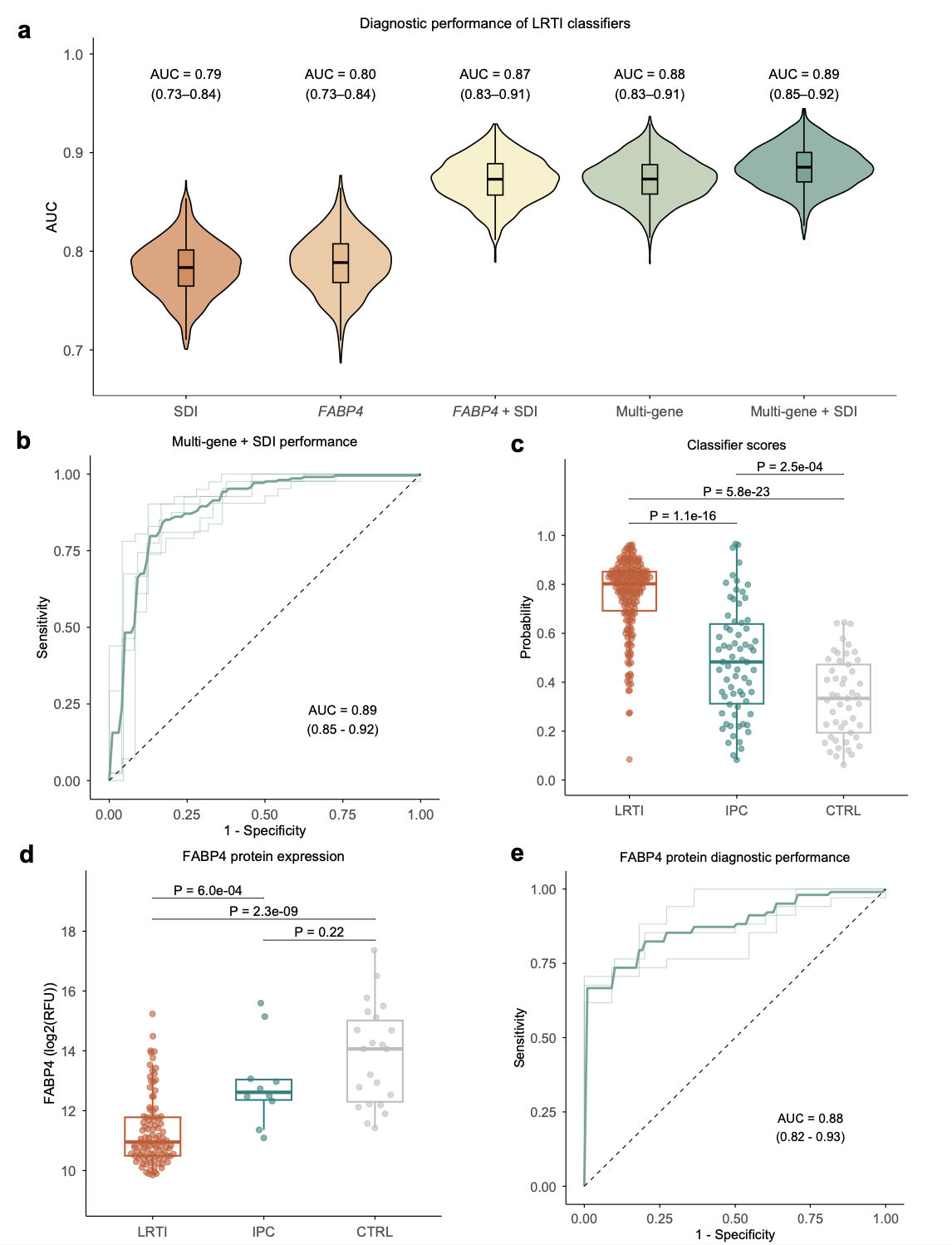
整合诊断模型的构建
基于上述发现,研究人员构建了诊断分类器。结果显示,单独的 FABP4 基因结合 Alpha 多样性指标即可达到 AUC 0.87;若整合多基因宿主转录谱与 Alpha 多样性,AUC 可达 0.89(95% CI 0.85-0.92)。在拥有蛋白数据的子集中,单独检测气道 FABP4 蛋白水平即实现了 AUC 0.88(95% CI 0.82-0.93)的优异性能,显示出其作为临床生物标志物的巨大潜力。
讨论
本研究揭示了 LRTI 和 IPC 截然不同的“宿主-微生物组原型”(Archetypes)。LRTI 本质上是病原体入侵导致的生态破坏(多样性崩溃)和强烈的免疫激惹;而 IPC 则表现为一种共生平衡态,即尽管病原体存在且微生物代谢活跃,但宿主并未触发显著的免疫防御程序。这种免疫反应的“衰减”或“耐受”可能是避免组织损伤的一种机制。
研究还证实,肺部微生物组的多样性本身就能调节免疫应答强度,高多样性环境可能抑制了过度的炎症反应。基于 FABP4 的诊断模型为临床提供了一种超越单纯病原检测的精准诊断思路,有助于减少抗生素滥用。
下呼吸道感染(LRTI)与无症状病原体携带(IPC)具有截然不同的微生物生态和免疫特征。LRTI 表现为微生物多样性降低和强烈的免疫激活,而 IPC 则维持了较高的微生物多样性和代谢活性,且宿主免疫反应静默。整合宿主基因 FABP4 与微生物 Alpha 多样性的诊断策略,能够高精度地鉴别真性感染,为临床管理急性呼吸道疾病提供了数据驱动的新工具。